2. Уравнение изотермы химической реакции
Если реакция протекает обратимо, то ΔG = 0.
Если реакция протекает необратимо, то ΔG ≤ 0 и можно рассчитать изменение ΔG. 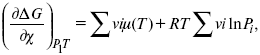
где χ – пробег реакции – величина, которая показывает, сколько молей изменилось в ходе реакции. I сп – характеризует равновесное и неравновесное состояние реакции, II сп – характеризует только неравновесные состояния.
Если
д χ = 1,
то 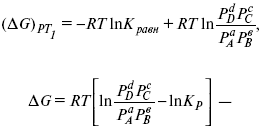
это уравнение изотермы химической реакции
. 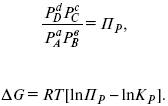
С помощью уравнения изотермы химической реакции можно судить о направлении протекания реакции.
1) Пp< Кp, ΔG < 0, слева направо;
2) Пp> Кp, ΔG > 0, справа налево;
3) Пp= Кp, ΔG = 0, химическое равновесие.
Смотрите также
Синтез изобутилового эфира уксусной кислоты реакцией этерификации
Изобутилацетат (изобутиловый эфир
уксусной кислоты) – бесцветная прозрачная жидкость с фруктовым запахом; хорошо
растворим в органических растворителях, ограниченно растворим в воде. Легко
...
Химия в хозяйстве
Земля как планета солнечной системы существует около
4,6 млрд. лет. Считают, что жизнь на ней зародилась 800—1000 тыс. лет назад.
Ученые обнаружили следы деятельности первобытного человека, ...
Основные типы химической связи
Вам известно, что атомы могут соединяться друг с
другом с образованием как простых, так и сложных веществ. При этом образуются
различного типа химические связи: ионная, ковалентная (неполярн ...
