1. Основные кинетические характеристики и методы их расчетов
i 0 – ток обмена – кинетическая характеристика равновесия между электродом и раствором при равновесном значении электродного потенциала. Токи обмена относят к 1 см2 поверхности раздела электрод-раствор.
α – коэффициент переноса заряда – характеризует степень влияния электрического поля электрода на энергию активации электрохимической стадии и определяет симметрию катодного и анодного процессов, зависит от формы потенциальных кривых.
α ≈ 0,5.
При одном и том же отклонении потенциала электрода от равновесного значения скорости реакции результативная плотность тока будет тем больше, чем выше i 0. Ток обмена i 0 зависит от природы электрохимической реакции, материала электрода и состава раствора.
Константа скорости
– скорость реакции при единичных концентрациях.
Скорость прямой реакции: 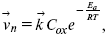
где k – константа, зависящая от свойств системы и способа выражения скорости процесса;
Cox – концентрация реагирующих частиц;
Ea – энергия активации разряда в отсутствии скачка потенциала между металлом и раствором.
Скорость обратной реакции 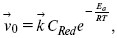
где CRed – концентрация частиц Red (восстановление продуктов);
Еa– энергия активации реакции ионизации при скачке потенциала между металлом и раствором, равным нулю.
Энергия активации электрохимического процесса зависит от величины электродного потенциала, природы ее непосредственных участников и электрода.
Энергия активации при постоянном перенапряжении η – эффективная энергия активации. Если энергия активации не зависит от перенапряжения, то ее появление замедляет диффузию.
Метод расчета величин α и i 0 основан на явлении редоксикинетического эффекта заключается в том, что при наложении переменного тока на электрод его потенциал смещается в ту или иную сторону на некоторую величину от первоначального значения. Это смещение – редоксикинетический потенциал
ψ. Связь редоксикинетического потенциала ψ с кинетическими параметрами а и i 0 такая: если наложить переменный ток на электрод, находящийся в равновесии с соответствующими ионами в растворе, то за время катодного полупериода он окажется заполяризованным катодно, причем зависимость между η и i при условии замедленности стадии разряда будет передаваться уравнением 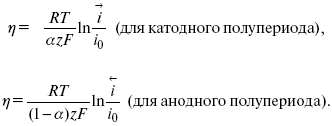
При достаточном удалении от состояния равновесия 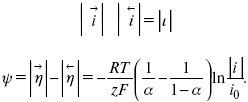
Из последнего выражения следует, если α= 0,5, то ψ = 0, чем сильнее α отклонена от 0,5, тем больше ψ.
Энергия активизации
– энергия, представляющая собой минимальную энергию, достаточную для осуществления акта химической реакции.
Смотрите также
Атомно-эмиссионный спектральный анализ
...
Современные и перспективные требования к дизельным топливам
В таблице 6 приведены требования
к качеству дизельных топлив по стандарту EN 590.
Приведена тенденция снижения серы, увеличения ЦЧ с 1993 по 2000 гг.
Таблица 6 — Требования к качеству дизель ...
Этанол
Спиртами
называются органические вещества, молекулы которых содержат одну или несколько
функциональных гидроксильных групп, соединенных с углеводородным радикалом.
Они могут
рассматр ...
