Термодинамика смесей идеальных газов. Характеристические функции идеального газа.
Для адиабатического процесса в системе (Q = 0) мы можем записать ΔU= -A.
Если идеальный газ расширяется адиабатически от объема V и температуры T до бесконечно большого объема, то он совершает работу:
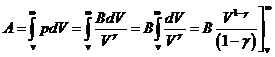 ,
,
а поскольку ![]() , то подстановка верхнего предела дает 0, подстановка нижнего приводит к
, то подстановка верхнего предела дает 0, подстановка нижнего приводит к 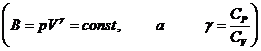 ,
,
![]() .
.
Следовательно ![]() , а поскольку
, а поскольку ![]() , то внутренняя энергия идеального газа, имеющего данную температуру, равна U = CVT.
, то внутренняя энергия идеального газа, имеющего данную температуру, равна U = CVT.
Очевидно, поскольку для идеального газа dU = CV dT, то по первому закону для идеального газа: dQ = CVdT + pdV.
Разделив правую и левую часть на Т, получим ![]() .
.
Интегрирование дает ![]()
![]() .
.
Константа интегрирования S0 не зависит ни от температуры, ни от давления или объема. Как мы увидим позднее для любого вещества в состоянии идеального газа в константу S0 в качестве характеристики вещества входит только его мольная масса. Далее:
H = U + pV = U + RT = CVT +RT = CpT,
F = U – TS = CVT – TS0 - CVT ln T –RT ln V,
G = H – TS = CpT – T( S0 + R ln R ) – CpT ln T + RT ln p,
Легко видеть, что, вообще говоря,
F = F (T) – RT ln V, G = G (T ) + RT ln p,
где F (T) и G (T) - являются функциями только температуры.
Смотрите также
Металловедение
Металловедение – наука,. Изучающая строение
и свойства металлов и устанавливающая связь между их составом, строением и
свойствами.
В данном реферате приведены общие и
теоретические сведе ...
Изучение взаимодействия в системе NaF-Bi2O3-BiF3 при 600 и 650 градусах Цельсия
Твердые
электролиты представляют собой вещества, проводящие электрический ток в твердом
состоянии, промежуточные в строении между твердыми кристаллическими телами с
фиксированным положением ...
Гетероциклические соединения
«Гетерос» -
по-гречески разный. Это циклические соединения, в кольца которых, кроме
углеродных атомов входят атомы других элементов, например, азота, серы,
кислорода (N,S,O)
и др. они наз ...
