Законы термохимии. Термохимические расчеты.
В основе термохимических расчетов лежит закон Гесса и его следствия.
В 1836г. Русский химик Гесс Г.И. экспериментально установил следующий закон:
· Тепловой эффект реакции (энтальпия реакции) при Vconst или Pconst не зависит от пути процесса (от числа промежуточных стадий), а определяется только начальным и конечным состоянием системы.
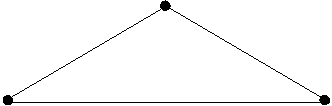
Наглядно этот закон можно показать на реакции образования СО2.
 |
![]()
![]()
![]() С + ½О2=СО СО + ½О2= СО2
С + ½О2=СО СО + ½О2= СО2
![]()
![]() ΔH0
ΔH0![]() I ΔH0
I ΔH0![]() II
II
С(гр.)+ О2 СО2(г.)
Исходное состояние ΔH0х.р. Конечное состояние
ΔH0х.р.=ΔH0I + ΔH0II; -393,5= -1105 - 283
С(графит) + О2= СО2; ΔH0= -393,5 кДж/моль
С(гр.) + ½О2(г.) =СО(г.); ΔH0I = -110,5 кДж/моль
СО(г.) + ½О2(г.)= СО2(г.); ΔH0II = -283 кДж/моль
Закон Гесса позволяет рассчитывать энтальпии отдельных стадий, которых экспериментально определить трудно. Так, из рассмотренного примера можно рассчитать энтальпию реакции окисления СО до СО2;
СО + ½О2= СО2, ΔH0II; ΔH0II = ΔH0 – ΔH0I= -393,5 – (-110,5)= -283 кДж/моль
Из закона Гесса вытекает ряд следствий. Некоторые из этих следствий раньше считались индивидуальными законами.
Рассмотрим два следствия из закона Гесса.
Смотрите также
Курсовая работа по органической химии
Актуальность
работы: В современной химии одной из актуальных проблем является синтез
биологически активных производных адамантана, которые в дальнейшем могут быть
использованы как лекарстве ...
Абсорбционная установка
Ключевые слова: УСТАНОВКА, АБСОРБЦИЯ,
КОЛОННА, РАСЧЕТ, ТЕХНОЛОГИЯ, АММИАК, ТАРЕЛКА.
В общей части
обсуждены современные методы извлечения компонентов из газовых смесей. Принята
абсорбцио ...
Энергетика ТЭК: Нефть, нефтяная промышленность
В данном реферате рассказывается о том, что
представляет собой нефть. Выссказаны различные мнения учёных об образовании
нефти. Отдельный раздел реферата посвящён рассмотрению вопросов получ ...
