Химические связи
Различают несколько типов химических связей: 1 – ионная. Ионная связь образуется при взаимодействии атомов, которые сильно различаются по электроотрицательности (связь между типичным металлом и типичным неметаллом).

Na0-1e = Na+ Cl0+1e = Cl—
Ионная связь характерна также для щелочей и солей, в которые входят кислород и активные металлы.
2 – ковалентная связь образуется при перекрывании электронных облаков.
Ковалентная неполярная образуется при взаимодействии атомов с одинаковыми электроотрицательностями.
![]()
Ковалентная полярная образуется при взаимодействии атомов, электроотрицательности которых различаются незначительно.
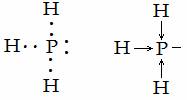
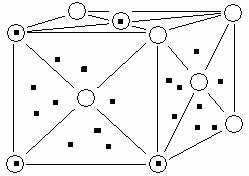
3 – металлическая связь образуется во всех металлах. Это связь, которую осуществляют относительно свободные электроны с положительными ионами металлов в кристаллической решётке. Атомы металла легко отдают валентные электроны и превращаются в положительные ионы. Относительно свободные электроны перемещаются между положительными ионами металла и между ними возникает металлическая связь, то есть электроны как бы цементируют положительные ионы металла в кристаллической решётке.
4 – водородная связь – это связь между атомом водорода одной молекулы и атомом сильного электроотрицательного элемента другой молекулы.
Водородная связь – это молекулярная связь. Она слабее, чем ионная и ковалентная связь.
Смотрите также
Программа для поступающих в вузы (ответы)
...
Углерод
Углерод
(лат. Carboneum), С - химический элемент IV группы периодической
системы Менделеева. Известны два стабильных изотопа 12С (98,892 %) и
13С (1,108 %).
Углерод известен с глубокой ...
Водные ресурсы
...
