Фенол
К фенолам относятся производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным ядром.
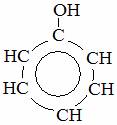
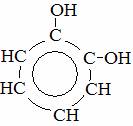
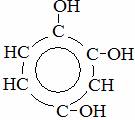
фенол 1,2-бензолдиол 1,2,4-бензолтриол
Строение молекулы фенола
Фенол является слабой кислотой.
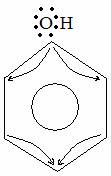
Физические свойства
Фенол – бесцветное, кристаллическое вещество с характерным запахом. Его t плавления = 40,9 С. В холодной воде он мало растворим, но уже при 70 С растворяется в любых отношениях. Фенол ядовит!
Химические свойства
I. Реакции, протекающие по гидроксильной группе
1) Взаимодействие с активными металлами
2C6H5OH + 2Na à 2C6H5ONa + H2![]()
фенолят натрия
2) Взаимодействие со щелочью
C6H5OH + NaOH à C6H5ONa + H2O
II. Реакции, протекающие по бензольному ядру. Реакции, протекающие по положениям 2, 4, 6.
1) Бромирование
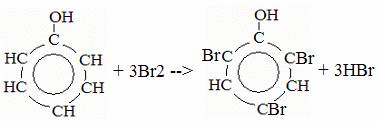
2,4,6-трибромфенол
2) Нитрование
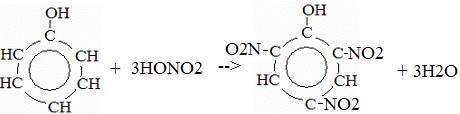
2,4,6-тринитрофенол
или пикриновая кислота
Получение
C6H6 à C6H5Cl à C6H5OH
1. C6H6 + Cl2 à C6H5Cl + HCl
2. C6H5Cl + NaOH à NaCl + C6H5OH
Применение
Получение лекарств, веществ для дезинфекции, фотореактивов, красителей, капрона, взрывчатых веществ, текстолита, гетинакса, карболита, стеклотекстолита, волокнита.
Смотрите также
Железо и его роль
Железо -
(лат. Ferrum), Fe (читается «феррум»), химический элемент, атомный номер 26,
атомная масса 55,847. Происхождение как латинского, так и русского названий
элемента однозначно не уста ...
Элементы статистической термодинамики
...
Платина
...
