Изучение свойств и эффективности функционирования ХТС
![]()
Вступает в альдольную конденсацию с образованием диацетонового спирта (СН3)2С(ОН)СН2СОСН3, а также в кротоновую конденсацию с образованием окиси мезитила (СН3)2С=СНСОСН3, форона (СН3)2С=СНСОСН=С(СН3)2 и мезитилена. В присутствии сильной минеральной кислоты ацетон алкилирует фенол с образованием дифенилолпропана (бисфенола ацетона) (НОС6Н4)2С(СН3)2, присоединяет цианид-ион с образованием ацетонциангидрина (CH3)2C(OH)CN. При пиролизе (700°С) ацетон образуются кетен СН2=С=О и метан. В промышленсти ацетон получают преимущественно так назеваемым кумольным способом одновременно с фенолом из бензола и пропилена через изопропилбензол (кумол) по схеме, рассмотренной подробнее выше:
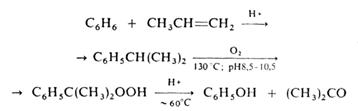
Ацетон - широко применяемый растворитель органических веществ, в первую очередь нитратов и ацетатов целлюлозы; благодаря сравнительно малой токсичности он используется также в пищевой и фармацевтической промышленности; ацетон служит также сырьем для синтеза уксусного ангидрида, кетена, диацетонового спирта, окиси, мезитила, метилизобутилкетона, метилметакрилата, дифенилолпропана, изофорона и многих других соединений. Для ацетон Твсп. -20°С, Тсамовоспл. 500°С; КПВ 2,15-13,00%. Ацетон при вдыхании накапливается в организме. Т.к. выводится из организма медленно, возможны хронические отравления. ПДК 200 мг/м3.
Смотрите также
Приложение 6
Подготовка нефти, включая
газовый конденсат, в тоннах
Российская Федераци 910610930
Западная Сибирь 708316453
Тюменская область ...
Полигалогенпроизводные алканов
...
Синтез этилового эфира 4-бромбенозойной кислоты
Цель работы состоит в
составление литературного обзора по спиртам и синтеза этилового эфира
4-бромбензойной кислоты.
Спиртами называются
органические вещества, молекулы которых содержат ...
