Классификация электродов
![]() .
.
В качестве индикаторных используют только мембранные электроды с К<1, такие электроды называют ионоселективными.
![]() ,
,
где КА-В - константа равновесия реакции обмена, в результате которой посторонние ионы ![]() проникают в фазу мембраны:
проникают в фазу мембраны:
AМZ+ + ![]() «
« ![]() + Aр-рZ+;
+ Aр-рZ+;
l (![]() ) и l(AZ+) - подвижности
) и l(AZ+) - подвижности ![]() и AZ+ ионов в фазе мембраны.
и AZ+ ионов в фазе мембраны.
Основными характеристиками ионоселективного электрода являются: интервал выполнения электродной функции, селективность и время отклика.
Интервал выполнения электродной функции относительно определяемого иона А+ характеризуется протяженностью линейного участка зависимости потенциала электрода от логарифма концентрации (активности) иона А.
Если зависимость имеет угловой коэффициент при 25°С, близкий к ![]() , то электрод выполняет нернстовскую функцию в данном интервале. Для лучших электродов нарушение нернстовской функции наблюдается только при СА < 10-7 моль/л. Точка перегиба на графике Е= f(
, то электрод выполняет нернстовскую функцию в данном интервале. Для лучших электродов нарушение нернстовской функции наблюдается только при СА < 10-7 моль/л. Точка перегиба на графике Е= f(![]() (A)) характеризует предел обнаружения А+ с помощью данного электрода (рис.2.).
(A)) характеризует предел обнаружения А+ с помощью данного электрода (рис.2.).
Селективность электрода относительно определяемого иона А в присутствии постороннего иона В характеризуется величиной КА, В. Если КА, В<1, то электрод селективен относительно иона А, а если КА, В >1, то относительно иона В. Для определения КА, В измеряют ЕМ в растворах с постоянным содержанием В и уменьшаемым А. При каком-то минимальном значении ра(А) линейный характер зависимости Е = f(ра(A)) нарушается (рис. 3.). Это означает, что потенциал электрода перестает зависеть от а(А), т.е. теряет электродную функцию от А и не отличает ио нов А от В. В точке пересечения линейных участков ЕА= ЕВ и при ZA = ZB: а(A) /а(B) = KA,B. Чем меньше КА, В, тем выше селективность электрода относительно иона А.
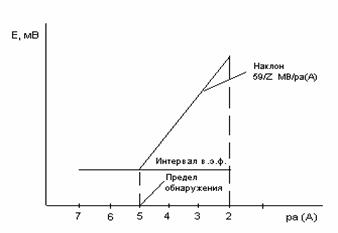
Рис. 2 Определение интервала выполнения электродной функции по графику зависимости Е = f(ра(A)).
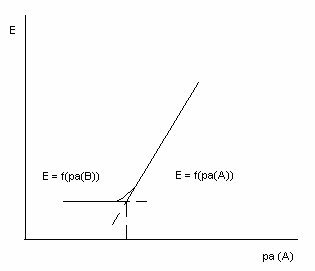
Рис. 3. Определение селективности электрода относительно вещества А по зависимости Е = f(ра (A)).
Время отклика ионоселективного электрода характеризует время достижения постоянного потенциала электрода. Чем меньше время отклика, тем лучше электрод. Оно может колебаться от секунд до минут. Это зависит от природы мембраны и методики проведения измерений (переносят ли электрод из разбавленного раствора в концентрированный или наоборот). Для большинства электродов потенциал в течение 1 мин. достигает 90% конечного значения.
Решением ИЮПАК условно принято считать величину ![]() = 0,00 В. Очевидно, что в этом случае измеренная величина ЭДС гальванического элемента, в состав которого входит водородный электрод, равна разности внутренних потенциалов второго электрода. Эту ЭДС принято называть электродным потенциалом или редоксипотенциалом и обозначать буквой Е. Переход от внутренних потенциалов к редоксипотенциалам не меняет характера формулы Нернста:
= 0,00 В. Очевидно, что в этом случае измеренная величина ЭДС гальванического элемента, в состав которого входит водородный электрод, равна разности внутренних потенциалов второго электрода. Эту ЭДС принято называть электродным потенциалом или редоксипотенциалом и обозначать буквой Е. Переход от внутренних потенциалов к редоксипотенциалам не меняет характера формулы Нернста:
![]() .
.
Для большинства электродов величина электродного потенциала при единичных активностях окисленной и восстановленной форм (Е0) измерена и приведена в справочниках.
При нормальных условиях и переходе от натуральных к десятичным логарифмам предлогарифмический множитель становится равным 0,0591, и формула приобретает вид
Смотрите также
Введение
Физическая химия – наука, объясняющая химические
явления и устанавливающая их закономерности на основе общих принципов физики.
Общая задача физической химии – предсказание
временного хода химичес ...
