Дипольный момент молекулы и связи
Представим себе, что можно найти “центры тяжести” отрицательных и положительных частей молекулы. Тогда условно все вещества можно разбить на две группы. Одну группу составляют те, в молекулах которых оба “центра тяжести” совпадают. Такие молекулы называются неполярными. К ним относятся все ковалентные двухатомные молекулы вида А2, а также молекулы, состоящие из трех и более атомов, имеющие высокосимметричное строение, например СО2, СS2 , СCl4 , С6 H6. Во вторую группу входят все вещества, у которых “центры тяжести” зарядов в молекуле не совпадают, молекулы которых характеризуются электрической асимметрией. Эти молекулы называют полярными. К ним относятся молекулы вида АВ, в которых элементы А и В имеют различную электроотрицательность, и многие более сложные молекулы. Систему из двух разноименных электрических зарядов, равных по абсолютной величине, называют диполем. Подробная информация купить спички у нас на сайте.
Полярность молекулы (и полярность связи) характеризуется дипольным моментом молекулы (или связи).
Величина дипольного момента сильно влияет на свойства полярных молекул и веществ, построенных из таких молекул. Полярные молекулы поляризуются в электрическом поле, устанавливаясь по силовым линиям поля, ориентируются в электических полях, создаваемых ионами в растворах, взаимодействуют между собой, замыкая свои электрические поля. Дипольный момент образуется за счет смещения центров положительного и отрицательного зарядов на некоторую величину l, называемую длиной диполя.
Чем более полярны молекулы, чем значительнее смещены валентные электронные пары к одному из атомов, тем больше m. И наоборот, если электрическая ассиметрия молекул незначительна, то величина m невлика .
Для системы из двух частиц дипольный момент m равен: m = el.
Где e- величина заряда;l- расстояние между центрами. Однако, определяя сразу величину дипольного момента, мы не знаем ни величины заряда e, локализованного в полярной молекуле, ни расстояния между центрами l.
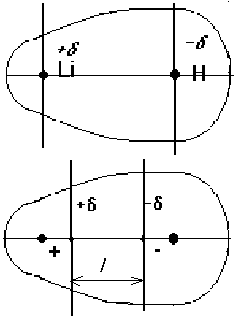
Принимаем e равным заряду электрона(1,6021*10-19Кл) и тогда получаем приведенную длину диполя l, которая является условной величиной. В качестве единицы измерения дипольных моментов принят дебай(названный в честь голландского физика П.Дебая, разработавшего теорию полярных молекул).в системе СИ 1D=0,33*10-29Кл*м.
Дипольные моменты обычно определяют экспериментально, измеряя относительную диэлектрическую проницаемость e веществ при различных температурах. Если вещество поместить в электрическое поле, создаваемое конденсатором, то емкость последнего возрастет в e раз, т.е. e=c/c0 (где c0 и с- емкость конденсатора в вакууме и в среде вещества).
Энергия электрического поля в конденсаторе U выражается соотношением:
U=1/2cV2,
где V- напряжение на обкладках конденсатора.
Из приведенного уравнения видно, что конденсатор в среде вещества имеет больший запас энергии, чем в вакууме (с>1). Это обусловлено тем, что под действием электрического поля происходит поляризация среды - ориентация диполей и деформация молекул. Первый эффект зависит от температуры, второй - не зависит.
Температурную зависимость относительно диэлектической проницаемости вещества e выражает уравнение Ланжевена-Дебая:
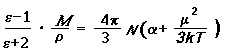 ’
’
где М- относительная молекулярная масса вещества; r- плотность вещества, NA- постоянная Авогадро; k- постоянная Больцмана, равная R/ NA (R- универсальная газовая постоянная); a- деформационная поляризуемость молекул.
Измерив e при двух температурах, с помощью уравнения Ланжевена-Дебая можно определить a и m. Есть и другие методы экспериментального определения m.
Значения дипольных моментов для некоторых связей между разнородными атомами приведены в таблице:

Не следует путать дипольный момент связи и дипольный момент молекулы, так как в молекуле могут существовать несколько связей, дипольные моменты которых суммируются как векторы.
Смотрите также
Синтез нанокристаллических полупроводниковых частиц
...
Стеклопластик
...
Альдегиды и кетоны
Это единения, содержащие
карбонильную группу = С = О . У альдегидов карбонил связан радикалом и
водородом. Общая формула альдегидов:
R
– C = O
H
У кетонов карбонил
связан ...
