Сера
Чистая сера представляет собой жёлтое кристаллическое вещество с плотностью 2,1 г/см3, плавящееся при 119 °С и кипящее при 445 °С. Она очень плохо проводит тепло и электричество. В воде сера нерастворима. Лучшим её растворителем является сероуглерод (СS2).
Элементарная сера существует при обычных условиях в виде восьмиатомных кольцевых молекул (рис. 2). Кристаллы образованные молекулами S8 имеют две формы. Ниже 95,4 °С устойчива обычная жёлтая сера с плотностью 2,07 г/см3, кристаллизующаяся в ромбической системе и имеющая т. пл. 112,8 °С (при быстром нагревании). Напротив, выше 95,4 °С устойчивы бледно-жёлтые кристаллы моноклинной серы с плотностью 1,96 г/см3 и т. пл. 119,3 °С (Sb) (рис. 3). Теплота превращения одной формы в другую составляет 3 кДж/моль. Интересно, что при трении сера приобретает сильный отрицательный заряд, а при охлаждении ниже -50 °С обесцвечивается.
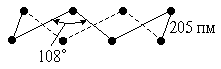

Рис. 2. Строение молекулы S8. Рис. 3. Диаграмма состояния серы.
В особых условиях удавалось получать для серы малоустойчивые разновидности и иных типов. Например, при замораживании (жидким азотом) сильно нагретых паров серы получается ее устойчивая лишь ниже -80 °С пурпурная модификация, образованная молекулами S2. Лучше других изучена форма, извлекаемая толуолом из подкисленного раствора Nа2S2O3. Ее оранжево-жёлтые кристаллы образованы кольцеобразными молекулами S6 [с параметрами d(SS) = 206 пм и ÐSSS = 102°]. Резким охлаждением насыщенного раствора серы в бензоле может быть получена состоящая из молекул S8 метастабильная ”перламутровая” модификация (Sg). Довольно сложным путем была получена форма, слагающаяся из циклических молекул S12 [d(SS) = 206 пм, ÐSSS = 106,5°]. Известны также формы, образованные молекулами S7 и S10.
Имеющиеся пока сведения о поведении серы при высоких давлениях неполны и отчасти противоречивы. Так, по одним данным, в области около 30 тыс. атм. и 300 °С формы кристаллов серы. устойчива кубическая фаза с плотностью 2,18 г/см3, по другим — в той же области устойчива обладающая ромбической решеткой “волокнистая” сера, слагающаяся из десятиатомных спиралей (с тремя оборотами на период 138 пм). Предполагается, что при 200 тыс. атм. сера может быть переведена в металлическое состояние.
Теплота плавления серы составляет 1,3 кДж/моль. Плавление сопровождается заметным увеличением объема (примерно на 15 %). Расплавленная сера представляет собой желтую легкоподвижную жидкость, которая выше 160 °С превращается в очень вязкую темно-коричневую массу. Как видно из рис. 4, около 190 °С вязкость серы примерно в 9000 раз больше, чем при 160 °С. Затем она начинает уменьшаться, и выше 300 °С расплавленная сера, оставаясь темно-коричневой, вновь становится легко подвижной.
Изменений физических свойств при нагревании связано с изменением внутреннего строения серы. Выше 160 °С кольца S8 начинают разрываться, причем концевые атомы возникающих открытых структур сцепляются друг с другом, образуя цепи с длиной до миллиона атомов, что сопровождается резким повышением вязкости (и изменением цвета). Дальнейшее нагревание ведет к быстрому уменьшению средней длины цепей, вследствие чего вязкость уменьшается (хотя все же остается значительно большей, чем ниже 160 °С). Работа разрыва цепи оценивается в 138 кДж/моль.
Температура кипения серы (444,7 °С) является одной из вторичных стандартных точек международной шкалы. Теплота испарения серы составляет 9,2 кДж/моль. В парах имеет место равновесие главным образом между молекулами S8, S6, S4 и S2, причем переход от S8 к S2 осуществляется эндотермически:
1/4S8 (+4,4 кДж) ® 1/3S6 (+29 кДж) ®1/2S4 (+58 кДж) ® S2
Поэтому по мере повышения температуры равновесие все более смещается вправо. Внешним признаком этого служит изменение цвета паров, которые вблизи точки кипения имеют оранжево-желтую окраску, при дальнейшем нагревании сначала краснеют, а затем начинают бледнеть и при 650 °С становятся соломенно-желтыми. Пары кипящей серы содержат (по объему) приблизительно 59 % S8, 34 % S6, 4 % S4 и 3 % S2 с небольшими примесями нечетных молекул (S3, S5, S7). По видимому, все эти молекулы Sn (кроме S2) имеют циклическое строение. Около 900 °С пары серы состоят практически только из молекул S2 [с расстоянием d(SS) = 189 пм]. Энергия их диссоциации на атомы равна 418 кДж/моль и заметной она становится приблизительно с 1500 °С. Теплота атомизации серы (при 25 °С) равна 272 кДж/моль.
По электронному строению молекула S2 подобна молекуле О2. Магнитные свойства последней указывают на наличие в ней двух неспаренных электронов.
|
Рис. 5. Вероятное строение цепи Sm. |
Смотрите также
Синтез метанола
...
Динамика полимерных цепей в процессах структурных и химических превращений макромолекул
Динамика
полимерных цепей в растворе характеризуется совокупностью релаксационных
процессов, связанных с движением (вращательным или поступательным)
макромолекулы как целого или тех или ины ...
Полимеры
Литературный обзор
Получение
слоистых пластиков связано с изготовлением на разных этапах технологического
процесса слоистых наполнителей – тканей, бумаг, шпона - поверхность которых
по ...

