Подгруппа хрома.
Безводный хлорид хрома (III) СrСl3 образуется в результате взаимодействия элементов при нагревании (теплота образования 510 кДж/моль). Он представляет собой красно-фиолетовые кристаллы, довольно легко возгоняющиеся в токе хлора. В воде СrСl3 (т. пл. 1150 °С) сам по себе практически нерастворим. Однако в присутствии следов СrСl2 или какого-либо другого сильного восстановителя растворение идет быстро и со значительным выделением тепла. Упариванием образующегося раствора из него может быть выделен легкорастворимый в воде темно-зелёный кристаллогидрат СrСl3·6Н2О. Известен и фиолетовый кристаллогидрат того же состава. Тёмно-зелёная форма гидролизована значительно сильнее фиолетовой. С хлоридами Сs¸Li хромтрихлорид способен образовывать кристаллические двойные соединения, примером которых может служить розово-красный СrСl3·3КСl (т. пл. 838 °С). Теплоты их образования из исходных молекул последовательно возрастают по ряду (кДж/моль): -2,9 (Nа), +46,0 (K), 68,9 (Rb), 76,9 (Сs). Весьма близко к СrСl3 стоят по свойствам зелёный СrF3 (т. возг. 1200 °С), чёрные СrВr3 и СrI3.
Азотнокислый хром [Сr(NО3)3] образуется при растворении Сr(ОН)3 в азотной кислоте. Его раствор имеет в отражённом свете сине-фиолетовую, а в проходящем — красную окраску. При нагревании он зеленеет, но при охлаждении первоначальный цвет довольно быстро восстанавливается. Кристаллизуется Сr(NО3)3 в зависимости от условий с различным числом молекул воды.
Безводный сульфат хрома Сr2(SO4)3, подобно хлориду, растворяется в воде только при одновременном наличии следов какого-либо сильного восстановителя. Из раствора он выделяется обычно в виде фиолетового кристаллогидрата Сr2(SO4)3·18Н2О. Известны также более бедные водой зелёные кристаллогидраты, например Сr2(SO4)3·6Н2О. При совместной кристаллизации сернокислого хрома с сульфатами некоторых одновалентных катионов (Nа+, К+, Rb+, Сs+, NН4+, Тl+) выделяются тёмно-фиолетовые кристаллы хромовых квасцов, отвечающие составу: М2SO4·Сr2(SO4)3 24Н2О. Из них хорошо растворимые в воде (около 1:4 по массе при обычных условиях) калийные квасцы применяются в кожевенной промышленности. Помимо квасцов известно зелёное кристаллическое соединение сульфата хрома с серной кислотой состава Сr2(SO4)3·Н2SO4·14Н2О. Получены были и некоторые аналогичные производные селеновой кислоты.
Сульфат хрома Сr2S3 в водных растворах не образуется, но может быть получен сухим путем, например пропусканием сероводорода над раскаленным хлоридом хрома. Сернистый хром представляет собой черное кристаллическое вещество, практически нерастворимое в воде и лишь медленно разлагаемое ею. Отвечающий ему тиохромит натрия (NаСrS2) может быть получен сплавлением хромита с содой и серой. Известны также тиохромиты ряда двухвалентных металлов.
Для хрома довольно характерно образование некоторых хромит-хроматных производных. Так, при взаимодействии растворимых соединений СrIII и СrVI в нейтральной среде выпадает коричневый осадок хромитхромата [Сr(ОН)2]НСrO4, при длительном промывании водой переходящий в [Сr(ОН)]СrO4. Коричневый Сr2(СrO4)3, (т. е. суммарно Сr5О12) образуется в водном слое при извлечении пероксида хрома эфиром. Нагреванием смесей бихромата с хромовым ангидридом могут быть получены нерастворимые в воде чёрные соли щелочных металлов суммарного состава МCr3О8, отвечающие структуре МСr(СrO4)2.
Весьма характерным для производных Сr3+ является образование двойных соединений с аммиаком, примером которых может служить фиолетовый СrCl3·6NН3. Соединения эти в твёрдом состоянии довольно устойчивы, а водой частично разлагаются с выделением осадка Сr(ОН)3 по уравнению, например:
СrCl3·6NH3 + 6 H2O Û Сr(ОН)3 + 3 NН4OН + 3 NН4Сl
Напротив, при наличии в растворе избытка аммиака и хлористого аммония равновесие смещается влево, т. е. в сторону растворения Сr(ОН)3 с образованием СrСl3·6NН3.
|
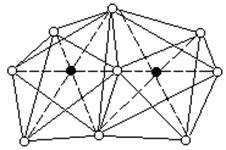
Рис. 5. Схема строения иона [W2Cl9]3–. |
Смотрите также
Промышленные синтезы на основе углеводородов
Углерод
определяется тем, что свыше 90 % всех первичных источников потребляемой в мире
энергии приходится на органическое топливо, главенствующая роль которого
сохранится и на ближайшие дес ...
Нитрование ароматических углеводородов. Производство нитро-бензола
Нитрования –
один из важнейших процессов в химической промышленности. Продукты, получаемые
за счёт нитрования, являются полуфабрикатами для производства многих товаров
различных ...
Определение массы полимера криоскопическим способом
Мы
выбрали тему – «Определение молекулярной массы вещества криоскопическим
методом». Изучая высокомолекулярные соединения, мы отметили, что их важной
характеристикой является молекулярная м ...