Сера
3 S + 6 NаОН = Nа2SO3 + 2 Nа2S + 3 Н2О
Находящаяся в избытке сера присоединяется затем к Nа2SO3, образуя гипосульфит. Параллельно происходит и образование полисульфидов натрия, сообщающих раствору желтый цвет. Для их разрушения с образованием гипосульфита в раствор пропускают SO2 до исчезновения желтой окраски жидкости.
Другой интересный способ получения гипосульфита основан на непосредственном взаимодействии SO2 и Н2S в щелочной среде. Если смесь обоих газов пропускать при сильном размешивании в раствор NаОН до его нейтрализации, то образуется гипосульфит:
4 SO2 + 2 Н2S + 6 NаОН = 3 Nа2S2O3 + 5 Н2О
При 48,5 °С гипосульфит плавится в своей кристаллизационной воде и около 100 °С теряет воду. Дальнейшее нагревание соли выше 220 °С сопровождается распадом, который идет в основном по схемам:
4 Nа2S2О3 = 3 Nа2SO4 + Nа2S5 Na2S5 = Nа2S + 4 S
Расплавленный гипосульфит очень склонен к переохлаждению. Иногда им пользуются как средой для определения молекулярных весов по понижению точки замерзания (криоскопическая константа 4,26 град). Из других тиосульфатов наиболее интересен малорастворимый (2 г/л) ВаS2O3, обменным разложением которого с сульфатами различных металлов удобно пользоваться для получения их тиосульфатов.
Подобно свободному хлору, другие сильные окислители (НОСl, Br2 и т. п.) окисляют гипосульфит до серной кислоты и ее солей. Иначе, а именно с образованием соли тетратионовой кислоты, протекает окисление гипосульфита сравнительно слабыми (или медленно действующими) окислителями, в частности иодом:
I2 +2 Nа2S2O3 = 2 NаI + Nа2S4O6
Эта реакция имеет большое значение для аналитической химии, так как служит основой одного из важнейших методов объемного анализа — так называемой иодометрии. Следует отметить, что в щелочной среде окисление гипосульфита иодом может протекать и до сульфата.
Медицинское применение гипосульфита довольно разнообразно. Его принимают внутрь (или вводят внутривенно) при отравлениях тяжелыми металлами, мышьяком и цианидами, а также для дезинфекции кишечника. Наружное (или внутреннее) применение показано при тяжелых ожогах и воспалениях кожи. Для лечения чесотки кожу больного повторно натирают концентрированным раствором Na2S2O3 и затем разбавленным раствором соляной кислоты.
Ближайшими аналогами Н2S2О3 являются политиосерные кислоты H2SnO3 (где n = 3¸7), которые могут быть получены в эфирной среде при -78 °С по общей схеме:
Н2Sn + SO3 + (С2Н5)2O = Н2Sn+1О3·(С2Н5)2O
Они хорошо растворимы в эфире и обладают сильно выраженными кислотными свойствами, но лишь одноосновны (в отличие от Н2S2О3), что соответствует строению сульфанмоносульфоновых кислот Н-Sn-1-SO2OН. И сами кислоты, и их соли разлагаются водой.
Для самого сернистого газа процессы, ведущие к повышению валентности серы, протекают значительно труднее, чем для сернистой кислоты и её солей. Наиболее важными из подобных реакций являются взаимодействия SO2 с хлором и кислородом.
С хлором диоксид серы непосредственно соединяется (на прямом солнечном свету) по реакции:
SO2 + Cl2 = SO2Cl2 + 92 кДж
Образующийся хлористый сульфурил представляет собой бесцветную жидкость с резким запахом. Холодная вода действует на него лишь медленно, но горячей он быстро разлагается с образованием серной и соляной кислот:
SO2Cl2 + 2 H2O = H2SO4 + 2 HСl
Вещество, дающее при взаимодействии с водой смесь галогенводородной и какой-либо другой кислоты, называется галогенангидридом последней. Хлористый сульфурил является, следовательно, хлорангидридом серной кислоты.
Если хлористый сульфурил можно рассматривать как серную кислоту, в которой на хлор заменены оба гидроксила, то продуктом подобного же замещения только одного из них является хлорсульфоновая кислота:
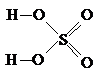
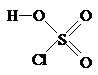
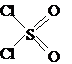
серная кислота хлорсульфоновая кислота хлористый сульфурил
Она может быть получена прямым соединением SO3 c HСl и, подобно хлористому сульфурилу, представляет собой бесцветную жидкость с резким запахом. Водой хлорсульфоновая кислота HSO3Cl бурно разлагается на HCl и H2SO4. Как и хлористый сульфурил, она находит применение при органических синтезах.
Хорошим катализатором при синтезе хлористого сульфурила (т. пл. -54, т. кип. 69 °С) является камфора. Молекула О2SСl2 полярна, ее пространственное строение отвечает неправильному тетраэдру с параметрами d(SO)) = 141 пм, ÐOSO = 123°, d(SСl) = 201 пм, ÐСlSСl = 100°. При нагревании выше 300 °С хлористый сульфурил распадается на SO2 и Сl2. Он является хорошим растворителем для SО3 и большинства хлоридов многовалентных металлов. Взаимодействие подобных растворов может служить удобным методом получения соответствующих безводных сульфатов. Известны также полисульфурилхлориды общей формулы SnO3n-1Cl2 с n = 2 ( т. пл. -37, т. кип. 152 °С), n = 3 (т. пл. -19 °С) и n = 4 (бесцветная жидкость).
Смотрите также
Элементарная биохимия
БИОХИМИЯ (биологическая химия) – биологическая наука, изучающая
химическую природу веществ, входящих в состав живых организмов, их превращения
и связь этих превращений с деятельностью органо ...
Климатические воздействия и их характеристики. Радиационные воздействия их характеристика
...
Биография и научная деятельность Юстуса Либиха
(1803-1873)
...
